Сінільная кіслата: Розніца паміж версіямі
| [дагледжаная версія] | [дагледжаная версія] |
Artsiom91Bot (размовы | уклад) др аўтаматычнае выдаленне шаблонаў стабаў |
VladimirZhV (размовы | уклад) Няма тлумачэння праўкі |
||
| Радок 39: | Радок 39: | ||
| ЛД50 = мышы (пэраральна) 3.7 |
| ЛД50 = мышы (пэраральна) 3.7 |
||
| таксічнасць = {{NFPA 704 |
| таксічнасць = {{NFPA 704 |
||
| |
| небяспека для здароўя = 4 |
||
| |
| вогненебяспечнасць = 4 |
||
| рэакцыяздольнасць = 1 |
|||
| реакционоспособность = 1 |
|||
| іншае = |
|||
| прочее = |
|||
}} |
}} |
||
| вугал Брустара = |
| вугал Брустара = |
||
| Радок 56: | Радок 56: | ||
| цвёрдасць = |
| цвёрдасць = |
||
}} |
}} |
||
'''Сіні́льная (цыяніставадародная) кіслата''', '''цыяністы вадарод''', '''нітрыл мурашынай кіслаты, HCN''' |
'''Сіні́льная (цыяніставадародная) кіслата''', '''цыяністы вадарод''', '''нітрыл мурашынай кіслаты, HCN''' — аднаасноўная [[кіслата]]. Адкрыта ў 1782 годзе шведскім [[хімік]]ам [[Карл Вільгельм Шэеле|К. В. Шэеле]], у 1811 годзе [[Жазеф Луі Гей-Люсак|Ж. Л. Гей-Люсак]] атрымаў бязводную сінільную кіслату і вызначыў яе склад<ref name="bse">{{З ВСЭ|Синильная кислота|}}</ref>. |
||
Бескаляровая, вельмі лятучая, лёгкарухомая атрутная [[вадкасць]] з характэрным пахам горкага міндалю. [[Тэмпература кіпення]] 25,65 [[Градус Цэльсія|°C]], [[шчыльнасць]] 687,08 кг/м³. Сумесь пары з [[паветра]]м (4,9—39,7 |
Бескаляровая, вельмі лятучая, лёгкарухомая атрутная [[вадкасць]] з характэрным пахам горкага міндалю. [[Тэмпература кіпення]] 25,65 [[Градус Цэльсія|°C]], [[шчыльнасць]] 687,08 кг/м³. Сумесь пары з [[паветра]]м (4,9—39,7 % кіслаты) выбуханебяспечная. Змешваецца ва ўсіх адносінах з [[вада|вадой]], [[этанол]]ам, дыэтылавым эфірам. Узаемадзейнічае з [[аксід]]амі і [[гідраксід]]амі [[Шчолачныя металы|шчолачных]] і [[Шчолачназямельныя металы|шчолачназямельных]] металаў. Не ўзаемадзейнічае з карбанатамі. |
||
Сінільная кіслата ўтрымліваецца ў некаторых [[Расліны|раслінах]], [[кокс]]авым газе, [[Тытунь|тытунёвым]] дыме, вылучаецца пры тэрмічным раскладанні [[нейлон]]у, поліурэтанаў. |
Сінільная кіслата ўтрымліваецца ў некаторых [[Расліны|раслінах]], [[кокс]]авым газе, [[Тытунь|тытунёвым]] дыме, вылучаецца пры тэрмічным раскладанні [[нейлон]]у, поліурэтанаў. |
||
З металамі ўтварае [[солі]] |
З металамі ўтварае [[солі]] — цыяніды. [[Арганічныя рэчывы|Арганічныя]] вытворныя сінільнай кіслаты маюць назву [[нітрылы]]. |
||
Асноўны метад атрымання ў [[Прамысловасць|прамысловасці]] |
Асноўны метад атрымання ў [[Прамысловасць|прамысловасці]] — акісляльны [[аманоліз]] [[метан]]у пры тэмпературы 1000 °C на каталізатары ([[Плаціна (хімічны элемент)|плаціна]], [[Сплаў|сплавы]] плаціны з [[Родый|родыем]] і плаціны з [[Ірыдый|ірыдыем]])<ref name="ch">[http://www.xumuk.ru/encyklopedia/2/4076.html ''Смирнов С. К.'' Синильная кислота] {{ref-ru}}</ref>. |
||
Сінільная кіслата выкарыстоўваецца у вытворчасці [[Цыяніды|цыянідаў]], |
Сінільная кіслата выкарыстоўваецца у вытворчасці [[Цыяніды|цыянідаў]], [[хлорцыян]]у, акрылатаў, [[Амінакіслоты|амінакіслот]], у якасці фуміганта і інш. |
||
{{зноскі}} |
{{зноскі}} |
||
| Радок 73: | Радок 73: | ||
* {{кніга|загаловак=Беларуская энцыклапедыя: У 18 т. Т.14: Рэле — Слаявіна|адказны=Рэдкал.: Г. П. Пашкоў і інш|месца=Мн.|выдавецтва=БелЭн|год=2002|том=14|старонкі=400|старонак=512|isbn=985-11-0238-5 (Т. 14)|тыраж=10 000}} |
* {{кніга|загаловак=Беларуская энцыклапедыя: У 18 т. Т.14: Рэле — Слаявіна|адказны=Рэдкал.: Г. П. Пашкоў і інш|месца=Мн.|выдавецтва=БелЭн|год=2002|том=14|старонкі=400|старонак=512|isbn=985-11-0238-5 (Т. 14)|тыраж=10 000}} |
||
* {{кніга|загаловак=Хімічны слоўнік навучэнца: Дапам. для вучняў|адказны=Б. Н. Качаргін, В. М. Макарэўскі, Л. Я. Гарнастаева, В. С. Аранская|месца=Мн.|выдавецтва=Народная асвета|год=2003|старонкі=214|старонак=287|isbn=985-12-0621-8|тыраж=1000}} |
* {{кніга|загаловак=Хімічны слоўнік навучэнца: Дапам. для вучняў|адказны=Б. Н. Качаргін, В. М. Макарэўскі, Л. Я. Гарнастаева, В. С. Аранская|месца=Мн.|выдавецтва=Народная асвета|год=2003|старонкі=214|старонак=287|isbn=985-12-0621-8|тыраж=1000}} |
||
* {{З ВСЭ|Синильная кислота|}} |
|||
| ⚫ | |||
== Спасылкі == |
== Спасылкі == |
||
* [http://www.xumuk.ru/encyklopedia/2/4076.html ''Смирнов С. К.'' Синильная кислота] {{ref-ru}} |
* [http://www.xumuk.ru/encyklopedia/2/4076.html ''Смирнов С. К.'' Синильная кислота] {{ref-ru}} |
||
* [http://slovari.yandex.ru/~книги/БСЭ/Синильная%20кислота/ Синильная кислота] // [[Вялікая савецкая энцыклапедыя]] {{ref-ru}} |
|||
| ⚫ | |||
{{Баявыя атрутныя рэчывы}} |
{{Баявыя атрутныя рэчывы}} |
||
Версія ад 13:15, 12 верасня 2020
| Сінільная кіслата | |
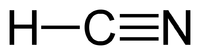
| |

| |

| |
| Агульныя | |
|---|---|
| Традыцыйныя назвы | цыянавадарод, сінільная кіслата |
| Хім. формула | HCN |
| Фізічныя ўласцівасці | |
| Стан (ст. ум.) | бясколерны газ ці бясколерная легкалятучая вадкасць |
| Малярная маса | 27,0253 г/моль |
| Шчыльнасць | 0,687 г/см³ |
| Дынамічная вязкасць (ст. ум.) | 0,201 Па·с (пры 20 °C) |
| Тэрмічныя ўласцівасці | |
| Тэмпература плаўлення | -13,4 °C |
| Тэмпература кіпення | 26,7 °C |
| Тэмпература ўспышкі | -17,8 °C |
| Малярная цеплаёмістасць (ст. ум.) | (сярэдняя для газу і вадкасці) 1,97 Дж/(моль·К) |
| Хімічныя ўласцівасці | |
| pKa | 9,21 |
| Растваральнасць у вадзе | у любых прапорцыях |
| Аптычныя ўласцівасці | |
| Паказчык пераламлення | 1,2675 |
| Структура | |
| Дыпольны момант | 2,98 Д |
| Класіфікацыя | |
| Рэг. нумар CAS | |
| PubChem | |
| Рэг. нумар EINECS | 200-821-6 |
| SMILES | |
| Рэг. нумар EC | 200-821-6 |
| RTECS | MW6825000 |
| ChemSpider | |
| Бяспека | |
| ЛД50 | мышы (пэраральна) 3.7 мг/кг |
| Таксічнасць | |
Сіні́льная (цыяніставадародная) кіслата, цыяністы вадарод, нітрыл мурашынай кіслаты, HCN — аднаасноўная кіслата. Адкрыта ў 1782 годзе шведскім хімікам К. В. Шэеле, у 1811 годзе Ж. Л. Гей-Люсак атрымаў бязводную сінільную кіслату і вызначыў яе склад[1].
Бескаляровая, вельмі лятучая, лёгкарухомая атрутная вадкасць з характэрным пахам горкага міндалю. Тэмпература кіпення 25,65 °C, шчыльнасць 687,08 кг/м³. Сумесь пары з паветрам (4,9—39,7 % кіслаты) выбуханебяспечная. Змешваецца ва ўсіх адносінах з вадой, этанолам, дыэтылавым эфірам. Узаемадзейнічае з аксідамі і гідраксідамі шчолачных і шчолачназямельных металаў. Не ўзаемадзейнічае з карбанатамі.
Сінільная кіслата ўтрымліваецца ў некаторых раслінах, коксавым газе, тытунёвым дыме, вылучаецца пры тэрмічным раскладанні нейлону, поліурэтанаў.
З металамі ўтварае солі — цыяніды. Арганічныя вытворныя сінільнай кіслаты маюць назву нітрылы.
Асноўны метад атрымання ў прамысловасці — акісляльны аманоліз метану пры тэмпературы 1000 °C на каталізатары (плаціна, сплавы плаціны з родыем і плаціны з ірыдыем)[2].
Сінільная кіслата выкарыстоўваецца у вытворчасці цыянідаў, хлорцыяну, акрылатаў, амінакіслот, у якасці фуміганта і інш.
Зноскі
- ↑ [Синильная кислота (руск.)] — артыкул з Вялікай савецкай энцыклапедыі
- ↑ Смирнов С. К. Синильная кислота (руск.)
Літаратура
- Беларуская энцыклапедыя: У 18 т. Т.14: Рэле — Слаявіна / Рэдкал.: Г. П. Пашкоў і інш. — Мн.: БелЭн, 2002. — Т. 14. — С. 400. — 512 с. — 10 000 экз. — ISBN 985-11-0238-5 (Т. 14).
- Хімічны слоўнік навучэнца: Дапам. для вучняў / Б. Н. Качаргін, В. М. Макарэўскі, Л. Я. Гарнастаева, В. С. Аранская. — Мн.: Народная асвета, 2003. — С. 214. — 287 с. — 1 000 экз. — ISBN 985-12-0621-8.
- [Синильная кислота (руск.)] — артыкул з Вялікай савецкай энцыклапедыі
- Синильная кислота // Российская энциклопедия по охране труда: В 3 т. — 2-е изд., перераб. и доп. — М.: Изд-во НЦ ЭНАС,2007. (руск.)
Спасылкі
- Смирнов С. К. Синильная кислота (руск.)

