Серная кіслата: Розніца паміж версіямі
| [дагледжаная версія] | [дагледжаная версія] |
Змесціва выдалена Змесціва дададзена
Luckas-bot (размовы | уклад) др r2.7.1) (робат дадаў: oc:Acid sulfuric |
др r2.7.1) (робат змяніў: pl:Kwas siarkowy |
||
| Радок 133: | Радок 133: | ||
[[no:Svovelsyre]] |
[[no:Svovelsyre]] |
||
[[oc:Acid sulfuric]] |
[[oc:Acid sulfuric]] |
||
[[pl:Kwas siarkowy |
[[pl:Kwas siarkowy]] |
||
[[pnb:گندھک دا تیزاب]] |
[[pnb:گندھک دا تیزاب]] |
||
[[pt:Ácido sulfúrico]] |
[[pt:Ácido sulfúrico]] |
||
Версія ад 16:44, 20 снежня 2011
| Серная кіслата | |
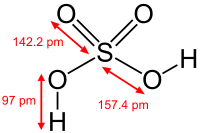
| |

| |

| |
| Агульныя | |
|---|---|
| Сістэматычнае найменне | серная кіслата |
| Хім. формула | H2SO4 |
| Фізічныя ўласцівасці | |
| Стан (ст. ум.) | вадкасць |
| Адн. малек. маса | 98,082 а. а. м. |
| Малярная маса | 98,082 г/моль |
| Шчыльнасць | 1,8356 г/см³ |
| Тэрмічныя ўласцівасці | |
| Тэмпература плаўлення | -10,38*З °C |
| Тэмпература кіпення | 279,6*З °C |
| Тэмпература ўзгарання | не ўзгарэцца °C |
| Удзельная цеплыня плаўлення | 10,73 Дж/кг |
| Хімічныя ўласцівасці | |
| pKa | -3 |
| Аптычныя ўласцівасці | |
| Паказчык пераламлення | 1.397 |
| Структура | |
| Дыпольны момант | 2.72 Д |
| Класіфікацыя | |
| Рэг. нумар CAS | |
| PubChem | |
| Рэг. нумар EINECS | 231-639-5 |
| SMILES | |
| Рэг. нумар EC | 231-639-5 |
| RTECS | WS5600000 |
| ChemSpider | |
| Бяспека | |
| ЛД50 | 510 мг/кг |
| Таксічнасць |
|
Серная кіслата H2SO4 — моцная двухасноўная кіслата, якая адпавядае вышэйшай ступені акіслення серы (6). Пры звычайных умовах канцэнтраваная серная кіслата — цяжкая алеістая вадкасць без колеру і паху. У тэхніцы сернай кіслатой называюць яе сумесі з вадой, так і з серным ангідрыдам SO3. Калі малярныя адносіны SO3:H2O < 1, то гэта водны раствор сернай кіслаты, калі> 1, — раствор SO3 ў сернай кіслаце (олеум).


