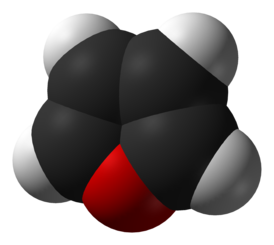
Фуран
| Фуран | |

| |
| |
| Агульныя | |
|---|---|
| Сістэматычнае найменне | фуран |
| Традыцыйныя назвы | фурфуран |
| Хім. формула | C4H4O |
| Фізічныя ўласцівасці | |
| Стан (ст. ум.) | вадкасць |
| Малярная маса | 68,07 г/моль |
| Шчыльнасць | 0,936 г/см³ |
| Тэрмічныя ўласцівасці | |
| Тэмпература плаўлення | -85,6 °C |
| Тэмпература кіпення | 31,4 °C |
| Аптычныя ўласцівасці | |
| Паказчык пераламлення | 1,4214 |
| Класіфікацыя | |
| Рэг. нумар CAS | |
| PubChem | |
| Рэг. нумар EINECS | 203-727-3 |
| SMILES | |
| ChemSpider | |
Фура́н — арганічнае злучэнне з формулай C4H4O. Пяцічленны гетэрацыкл з адным атамам кіслароду. Родапачынальнік вялікай групы арганічных злучэнняў, многія з якіх маюць практычнае значэнне, напрыклад фурфурол, тэтрагідрафуран, α-метылфуран (сільван).
Уяўляе сабой бескаляровую вадкасць з характэрным пахам, нагадваючым пах хлараформу. Малекулярная маса 68,07. Тэмпература плаўлення −85,65 °C. Тэмпература кіпення 31,83 °C. Шчыльнасць 0,937 г/см³ пры тэмпературы 20 °C. Добра раствараецца ў арганічных растваральніках, дрэнна раствараецца ў вадзе — утварае азеатропную сумесь (98,8 % фурану). Фуран устойлівы да ўздзеяння шчолачаў і раскладаецца кіслотамі. На паветры лёгка акісляецца.
Атрыманне[правіць | правіць зыходнік]
Фуран разам з сільванам утрымліваецца ў прадуктах сухой перагонкі драўніны некаторых парод. У лабараторных умовах атрымліваюць дэкарбакісліраваннем піраслізевай кіслаты. У прамысловых умовах фуран атрымліваюць дэкарбаніліраваннем фурфуролу.
Выкарыстанне[правіць | правіць зыходнік]
Фуран выкарыстоўваецца ў працэсах сінтэзу тэтрагідрафану, піролу, малеінавага ангідрыду, селенафену. Таксама выкарыстоўваецца ў якасці растваральніка алеяў і тлушчаў.
Шкоднае ўздзеянне[правіць | правіць зыходнік]
Фуран — таксічнае рэчыва. Пранікаючы праз непашкоджаную скуру, шкодна ўздзейнічае на печань і цэнтральную нервовую сістэму.
Літаратура[правіць | правіць зыходнік]
- Беларуская энцыклапедыя: У 18 т. Т. 16: Трыпалі — Хвіліна / Рэдкал.: Г. П. Пашкоў і інш. — Мн. : БелЭн, 2003. — Т. 16. — С. 504. — 10 000 экз. — ISBN 985-11-0035-8. — ISBN 985-11-0263-6 (т. 16).
- Хімічны слоўнік навучэнца: Дапаможнік для вучняў / Б. Н. Качаргін, В. М. Макарэўскі, Л. Я. Гарнастаева, В. С. Аранская. — Мн.: Народная асвета, 2003. — С. 250. — 287 с. — 1 000 экз. — ISBN 985-12-0621-8.
- Рабинович В. А., Хавин З. Я. Краткий химический справочник — Л.: Химия, 1977. (руск.)
Спасылкі[правіць | правіць зыходнік]
| Фуран на Вікісховішчы |
