Біяхімія
Біялагічная хімія, або біяхімія — навука аб хімічным складзе жывых клетак і арганізмаў і аб хімічных працэсах, якія ляжаць у аснове іх жыццядзейнасці. Навука вывучае структуру і функцыі кампанентаў клетак і рэчываў арганізма, як то бялкі, вугляводы, ліпіды, нуклеінавыя кіслоты і іншыя біямалекулы. Біяхімія імкнецца адказваць на біялагічныя і біяхімічныя пытанне з дапамогай хімічных метадаў.
Нягледзячы на тое, што існуе шырокі шэраг розных біямалекул, многія з іх з'яўляюцца палімерамі, гэта значыць складанымі вялікімі малекуламі, якія складаюцца з многіх падобных субадзінак, монамераў. Кожны клас палімерных біямалекул мае ўласны набор тыпаў гэтых субадзінак. Напрыклад, бялкі з'яўляюцца палімерамі, якія складаюцца з амінакіслот. Біяхімія вывучае хімічныя ўласцівасці важных біялагічных малекул, як то бялкі, у прыватнасці хімію рэакцый, каталізаваных ферментамі.
Акрамя таго, большая частка даследаванняў па біяхіміі мае справу з метабалізмам клеткі і яго эндакрыннай і паракрыннай рэгуляцыяй. Іншыя вобласці біяхіміі ўключаюць даследаванне генетычнага кода ДНК і РНК, біясінтэз бялкоў, транспарціроўку праз біялагічныя мембраны і перадачу сігналаў.
Класіфікацыя[правіць | правіць зыходнік]
Адрозніваюць біяхімію
- статычную, якая займаецца пераважна аналізам хімічнага саставу арганізмаў і цесна ўзаемазвязана з біяарганічнай хіміяй і малекулярнай біялогіяй,
- дынамічную, што даследуе працэсы ператварэння рэчываў у арганізме,
- функцыянальную, якая высвятляе сувязі паміж хімічнымі ператварэннямі малекул і функцыяй клеткі ці органа (механізмы сакрэцыі, мышачнае скарачэнне, перадача спадчынных уласцівасцяў і інш.), а таксама механізмы рэгуляцыі працэсаў жыццядзейнасці.
Паводле аб'ектаў даследавання адрозніваюць
- біяхімію мікраарганізмаў
- біяхімію раслін
- біяхімію жывёл
- біяхмію чалавека.
Шэраг разделаў біяхіміі вылучаюць у асобныя навуковыя дысцыпліны: біяхімія вітамінаў, гармонаў, клінічная біяхімія і інш.
Асобна ідуць параўнальная і эвалюцыйная біяхімія, якія займаюцца вывучэннем узаемасувязі паміж рознымі жывымі арганізмамі на малекулярным узроўні.
Гісторыя[правіць | правіць зыходнік]
Як асобная навука біяхімія сфарміравалася ў 19 стагоддзі.Тэрмін «біяхімія» эпізадычна ўжываўся з сярэдзіны XIX стагоддзя, але ў класічным сэнсе быў прапанаваны і ўведзены ў навуковае асяроддзе ў 1903 годзе нямецкім хімікам Карлам Нойбергам.
Гісторыя развіцця біяхіміі бярэ пачатак ад ятрахімікаў (нямецкі ўрач і прыродазнавец Парацэльс, 16 ст., і інш.), якія разглядалі жыццядзейнасць чалавека з пазіцый хіміі, увялі ў практыку лячэння шэраг хімічных прэпаратаў.
У пачатку 19 стагоддзя праведзены даследаванні па вывучэнні хімічнага саставу раслінных і жывёльных клетак, у 1828 годзе сінтэзавана мачавіна (нямецкі хімік Ф. Вёлер), у 1842 годзе ў Германіі выдадзены першы падручнік па біяхіміі (І. Зіман). Ва ўніверсітэтах Еўропы, Расіі (Казань, А. Я. Данілеўскі, 1863) адкрыты кафедры біяхіміі. У 2-й палове 19 стагоддзя назапашаны некаторыя звесткі пра састаў і хімічный пераўтварэнні бялкоў, тлушчу і вугляводаў, працэс браджэння (нямецкія вучоныя Ю. Лібэх, Э. Бухнер, французскі вучоны Л. Пастэр), фотасінтэз (К. А. Ціміразеў).
Вялікі ўклад у развіццё біяхіміі ў Расіі зрабілі М. В. Ненцкі, адзін з заснавальнікаў тэорыі біясінтэзу мачавіны ў арганізме млекакормячых, Я. С. Лондан (распрацаваў метады ангіястаміі і арганастаміі для прыжыццёвага даследавання абменных працэсаў на цэлыя арганізме), У. І. Паладзін і Дз. М. Пранішнікаў (вывучалі абмен азоту ў раслінах), А. М. Бах (заснавальнік школы рускіх біяхімікаў; даследаваў хімізм фотасінтэзу і акісляльныя працэсы ў клетцы) і інш.[1]
Новы штуршок развіццю біялагічнай хіміі далі работы па вывучэнню браджэння, ініцыяваныя Луі Пастэрам. У 1897 годзе Эдуард Бухнер даказаў, што ферментацыя цукру можа адбывацца ў прысутнасці бясклетачнага дражджавога экстракта, і гэты працэс не столькі біялагічны, колькі хімічны[2]. На мяжы XIX і XX стагоддзяў працаваў нямецкі біяхімік Э. Фішэр. Ён сфармуліраваў асноўныя палажэнні пептыднай тэорыі будовы бялкоў, вызначыў структуру і ўласцівасці амаль усіх амінакіслот, якія ўваходзіць у іх склад. Але толькі ў 1926 годзе Джэймсу Самнеру ўдалося атрымаць першы чысты фермент, урэазу, і даказаць, што фермент — гэта бялок[3].
Біяхімія стала першай біялагічнай дысцыплінай з развітым матэматычным апаратам дзякуючы працам Холдейна, Міхаэліса, Ментэн і іншых біяхімікаў, якія стварылі ферментатыўную кінетыку, асноўным законам якой з’яўляецца ўраўненне Міхаэліса-Ментэн[4].
У 1928 годзе Фрэдэрык Грыфіт упершыню паказаў, што экстракт забітых награваннем хваробатворных бактэрый можа перадаваць прыкмету патагеннасці бяспечным бактэрыям. Даследаванне трансфармацыі бактэрый у далейшым прывяло да ачыстцы хваробатворнага агента, якім, насуперак чаканням, апынуўся не бялок, а нуклеінавыя кіслата. Сама па сабе нуклеінавыя кіслата не з’яўляецца небяспечная, яна толькі пераносіць гены, якія вызначаюць патагеннасць і іншыя ўласцівасці мікраарганізма. У 1953 годзе амерыканскі біёлаг Дж. Уотсан і англійскі фізік Ф. Крык, абапіраючыся на працы М. Уілкінса і Р. Франклін, апісалі структуру ДНК — ключ да разумення прынцыпаў перадачы спадчыннай інфармацыі. Гэта адкрыццё азначала нараджэнне новага кірунку навукі — малекулярнай біялогіі[5].
У 1958 годзе Джордж Бідл і Эдуард Тэйтэм атрымалі Нобелеўскую прэмію за працу, праведзеную на грыбах, высновай якой стала гіпотэза «адзін ген — адзін фермент»[6]. У 1988 годзе Колін Пітчфорк стаў першым чалавекам, асуджаным за забойства на аснове доказаў, атрыманых у выніку ДНК-дактыласкапіі доказаў, і першым злачынцам, злоўленым ў выніку масавага прымянення працэдуры дактыласкапіі[7]. З апошніх вех у развіцці біяхіміі варта адзначыць атрыманне Эндру Фаерам і Крэйгам Мело Нобелеўскай прэміі па фізіялогіі і медыцыне за «адкрыццё РНК-інтэрферэнцыі — эфекту гашэння актыўнасці пэўных генаў»[8][9].
Метады[правіць | правіць зыходнік]
Аснову біяхімічнай метадалогіі складаюць фракцыянаванне, аналіз, вывучэнне структуры і ўласцівасцяў асобных кампанентаў жывога рэчыва. Метады біяхіміі пераважна фарміраваліся ў XX стагоддзі; найбольш распаўсюджанымі з'яўляюцца храматаграфія, вынайдзеная М. С. Цветам у 1903 годзе[10], цэнтрыфугаванне (Т. Сведберг, 1923 г., Нобелеўская прэмія па хіміі ў 1926 годзе) і электрафарэз (А. Тыселіус, 1937 г., Нобелеўская прэмія па хіміі ў 1948 годзе)[11][12].
З канца ХХ стагоддзя ў біяхіміі ўсё шырэй прымяняюцца метады малекулярнай і клетачнай біялогіі, у асаблівасці штучная экспрэсія і накаўт генаў у мадэльных клетках і цэлых арганізмах (гл. генная інжынерыя, біятэхналогія). Штучныя экспрэсія раней невядомых генаў дала біяхімікам новы матэрыял для даследаванняў, часта недаступны традыцыйнымі метадамі. У выніку паўстаў новы падыход да планавання біяхімічнага даследавання, які атрымаў назву адваротная генетыка, або функцыянальная геноміка[13]. У апошнія дзесяцігоддзі вялікае развіццё адбылося ў галіне камп'ютарнага мадэліравання. Гэта методыка дазваляе даследаваць ўласцівасці біямалекул там, дзе немагчыма (або вельмі цяжка) правесці прамы эксперымент. Методыка заснавана на камп'ютарных праграмах, якія дазваляюць візуалізаваць структуру біямалекул, задаць іх меркаваныя ўласцівасці і назіраць выніковыя інтэракцыі паміж малекуламі, такія як, напрыклад, энзім — субстрат, энзім — коэнзім, энзім — інгібітар[12].
Неабходныя хімічныя элементы[правіць | правіць зыходнік]
З 90 хімічных элементаў, якія сустракаюцца ў натуральным стане ў прыродзе, для падтрымання жыцця неабходна крыху больш за чвэрць. Большасць рэдкіх элементаў не з'яўляюцца неабходнымі для падтрымання жыцця (выключэннямі з'яўляюцца селен і ёд). Жывымі арганізмамі не выкарыстоўваюцца таксама два распаўсюджаных элемента — алюміній і тытан. Спісы неабходных для жывых арганізмаў элементаў адрозніваюцца на ўзроўні вышэйшых таксонаў. Усім жывёлам неабходны натрый, а некаторыя расліны абыходзяцца без яго. Раслінам неабходны бор і крэмній, а жывёлам — не (або неабходны ў невялікай колькасці). Усяго шэсць элементаў (так званыя макранутрыенты, або органагенные элементы) складаюць да 99 % ад масы чалавечага арганізма. Гэта вуглярод, вадарод, азот, кісларод, кальцый і фосфар. Акрамя гэтых шасці асноўных элементаў, чалавеку неабходны малыя або мікраскапічныя колькасці яшчэ 19 элементаў: натрый, хлор, калій, магній, сера, жалеза, фтор, цынк, крэмній, медзь, ёд, бор, селен, нікель, хром, марганец, малібдэн, кобальт[14] і, як паказана ў 2014 годзе, бром[15].
Біямалекулы[правіць | правіць зыходнік]
Чатыры асноўныя тыпы малекул, даследаваннем якіх займаецца біяхімія, — гэта вугляводы, ліпіды, бялкі і нуклеінавыя кіслоты, а таксама іх гібрыды, протэагліканы, глікапратэіны, ліпапратэіны і інш. Многія біямалекулы з'яўляюцца палімерамі. Біялагічныя палімеры часта складаюць комплексы, будова якіх дыктуецца іх біялагічнай функцыяй[12].
Вугляводы[правіць | правіць зыходнік]
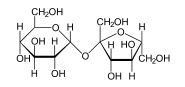
Вугляводы складаюцца з монамераў, або монацукрыдаў, як, напрыклад, глюкоза (C6H12O6), фруктоза (C6H12O6)[16], і дэзоксірыбоза (C5H10O4). Падчас сінтэзу малекулы дыцукрыда з двух малекул монацукрыдаў утвараецца малекула вады. Поліцукрыды служаць для акумуляцыі энергіі (крухмал ў раслін, глікаген у жывёл) і як структураўтваральныя малекулы (напрыклад, асноўным кампанентам клеткавых сценак раслін з'яўляецца поліцукрыд цэлюлоза, а хіцін з'яўляецца структурным поліцукрыдам ніжэйшых раслін, грыбоў і беспазваночных жывёл)[17].

Ліпіды[правіць | правіць зыходнік]
Ліпіды (тлушчы), як правіла, складаюцца з малекулы гліцэрына, да якой складана-эфірнай сувяззю мацуюцца ад адной (монагліцэрыды) да трох (трыгліцэрыды) тлустых кіслот. Тлустыя кіслоты дзеляцца на групы па даўжыні вуглевадароднага ланцуга і па ступені насычанасці (наяўнасці і колькасці падвойных сувязяў у ланцугу). Ліпіды ў жывёл служаць асноўнымі энергаёмістамі малекуламі. Акрамя таго, яны маюць розныя функцыі, звязаныя з перадачай клеткавых сігналаў і пераносу ліпафільных малекул[18].
Бялкі[правіць | правіць зыходнік]
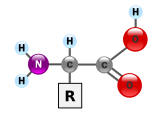
Бялкі, як правіла, з'яўляюцца буйнымі малекуламі — макрабіяпалімерамі. Іх монамерамі з'яўляюцца амінакіслоты. Большасць арганізмаў сінтэзуюць бялкі з 20 розных тыпаў амінакіслот. Амінакіслоты адрозніваюцца так званай R-групай, будова якой мае вялікае значэнне ў згортванні бялку ў трохмерную структуру. Амінакіслоты ўтвараюць паміж сабой пептыдныя сувязі, выбудоўваючы пры гэтым ланцужок — поліпептыд. Параўнанне паслядоўнасці амінакіслот у бялках дазваляе біяхімікам вызначыць ступень гамалагічнасці двух (ці больш) бялкоў[19].
Функцыі бялкоў у клетках жывых арганізмаў больш разнастайныя, чым функцыі іншых біяпалімераў — поліцукрыдаў і ДНК. Так, бялкі-ферменты каталізуюць праходжанне біяхімічных рэакцый і граюць важную ролю ў абмене рэчываў. Некаторыя бялкі выконваюць структурную або механічную функцыю, утвараючы цыташкілет, які падтрымлівае форму клетак. Таксама бялкі граюць ключавую ролю ў сігнальных сістэмах клетак, пры імунным адказе і ў клеткавым цыкле. Многія бялкі, як ферменты, так і структуральные бялкі, ствараюць комплексы з небялковых біямалекул. Комплексы з алігацукрыдамі называюцца (у залежнасці ад параўнальнай долі бялку і поліцукрыдаў у комплексе) глікапратэінамі або протэагліканамі. Комплексы з ліпідамі называюцца ліпапратэінамі[20].
Нуклеінавыя кіслоты[правіць | правіць зыходнік]
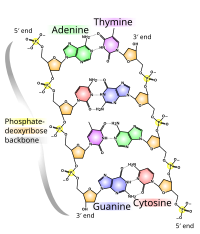
Нуклеінавая кіслата — гэта комплекс макрамалекул, які складаецца з полінуклеатыдных ланцужкоў. Асноўная функцыя нуклеінавых кіслот — захоўванне і кадаванне генетычнай інфармацыі. Нуклеінавыя кіслата сінтэзуецца з макраэргічных монануклеазідтрыфасфатаў (АТФ, ГТФ, ТТФ, ЦТФ, УТФ), адзін з якіх адэназінтрыфасфат (АТФ), з'яўляецца да таго ж асноўнай энергаёмістай малекулай усіх жывых арганізмаў. Самымі распаўсюджанымі нуклеінавымі кіслотамі з'яўляюцца дэзоксірыбануклеінавая кіслата (ДНК) і рыбануклеінавая кіслата (РНК). Нуклеінавыя кіслоты можна выявіць ва ўсіх жывых клетках ад архей да эукарыётаў, а таксама ў вірусах[21].
Назва «нуклеінавыя кіслоты» была дадзена гэтай групе біяпалімераў з-за іх асноўнага месцазнаходжання — у клеткавым ядры. Монамеры гэтых малекул называюцца нуклеатыдамі. Нуклеатыды складаюцца з трох кампанентаў: азоцістай асновы (пурына або пірымідзіна), монацукрыда тыпу пентозы і фасфатнай групы. ДНК і РНК адрозніваюцца паміж сабой тыпам пентозы (у ДНК гэта 2-дэзоксірыбоза, а ў РНК — рыбоза), а таксама магчымым складам азоцістых асноў (у той час як адэнін, гуанін і цытазін прысутнічаюць як у ДНК, так і ў РНК, тымін прысутнічае выключна ў ДНК, а ўрацыл — выключна ў РНК)[22].
Біяхімія ў Беларусі[правіць | правіць зыходнік]
На Беларусі біяхімічныя даследаванні праводзяцца з канца 19 стагоддзя. Цяпер вядуцца ў біялагічных інстытутах НАН РБ, НДІ медыцынскага і сельскагаспадарчага профілю, на адпаведных кафедрах і ў навуковых цэнтрах ВНУ.
Найбольш вядомы працы па біяхіміі фотасінтэзу (Ц. М. Годнеў, А. А. Шлык, А. С. Вечар), глебавых ферментаў (В. Ф. Купрэвіч), біяхіміі мікраэлементаў (В. А. Лявонаў, Ф. Я. Беранштэйн), вітамінаў (Ю. М. Астроўскі), біяхіміі біялагічных мембранаў (С. В. Конеў), па патахіміі (М. Ф. Меражынскі), біяхіміі апрамененага арганізма (Л. С. Чаркасава).
Зноскі
- ↑ БелЭн 1996, p. 181.
- ↑ Березов 1998, p. 17.
- ↑ The Nobel Prize in Chemistry 1946
- ↑ Chen, W.W.,Neipel, M., Sorger, P.K. (2010). "Classic and contemporary approaches to modeling biochemical reactions". Genes Dev. 24 (17): 1861–1875. doi:10.1101/gad.1945410. PMC 2932968. PMID 20810646.
{{cite journal}}: Папярэджанні CS1: розныя назвы: authors list (link) - ↑ Crick F. H., Barnett L., Brenner S., Watts-Tobin R. J. (1961). "General nature of the genetic code for proteins" (PDF reprint). Nature. 192: 1227–32. doi:10.1038/1921227a0. PMID 13882203.
{{cite journal}}: Невядомы параметр|month=ігнараваны (даведка)Папярэджанні CS1: розныя назвы: authors list (link) - ↑ Beadle G. W., Tatum E. L. (15 November 1941). "Genetic Control of Biochemical Reactions in Neurospora". PNAS. 27 (11): 499–506. doi:10.1073/pnas.27.11.499. PMC 1078370. PMID 16588492. Архіўная копія. Архівавана з першакрыніцы 24 верасня 2015. Праверана 12 студзеня 2015.[1]
- ↑ Butler, John M. (2009). Fundamentals of Forensic DNA Typing. Academic Press. p. 5. ISBN 978-0-08-096176-7.
- ↑ Andrew Fire, Siqun Xu, Mary K. Montgomery, Steven A. Kostas, Samuel E. Driver und Craig C. Mello: Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans. In: Nature. Band 391, 1998, S. 806—811, PMID 9486653 PDF Архівавана 12 студзеня 2006.
- ↑ Sen, Chandan K.; Roy, Sashwati (2007). "miRNA: Licensed to kill the messenger". DNA Cell Biology. 26 (4): 193–194. doi:10.1089/dna.2006.0567. PMID 17465885.
{{cite journal}}: Папярэджанні CS1: розныя назвы: authors list (link) - ↑ Березов 1998, p. 26.
- ↑ Березов 1998, p. 30-32.
- ↑ а б в Monique Laberge. Biochemistry. — USA: Infobase Publishing, 2008. — С. 4. — 112 с. — ISBN 97807910196932.
- ↑ Koonin E., Galperin M. Sequence — Evolution — Function.
- ↑ Ultratrace minerals. Authors: Nielsen, Forrest H. USDA, ARS Source: Modern nutrition in health and disease / editors, Maurice E. Shils … et al.. Baltimore : Williams & Wilkins, c1999., p. 283—303. Issue Date: 1999 URI: [2]
- ↑ McCall AS, Cummings CF, Bhave G, Vanacore R, Page-McCaw A, Hudson BG (2014). "Bromine Is an Essential Trace Element for Assembly of Collagen IV Scaffolds in Tissue Development and Architecture". Cell. 157 (6): 1380–92. doi:10.1016/j.cell.2014.05.009. PMID 24906154.
{{cite journal}}: Папярэджанні CS1: розныя назвы: authors list (link) - ↑ Whiting, G.C. Sugars // The Biochemistry of Fruits and their Products / A.C. Hulme. — London & New York: Academic Press. — Т. Volume 1. — С. 1–31.
- ↑ Н. А. Тюкавкина, Ю. И. Бауков. Биоорганическая химия. — 1-е изд. — М.: Медицина, 1985. — С. 349—400. — 480 с. — (Учебная литература для студентов медицинских институтов).
- ↑ Nelson D.L., Cox M.M. Lehninger Principles of Biochemistry. — 5th. — W. H. Freeman, 2008. — ISBN 978-0-7167-7108-1.
- ↑ Общая биология. Учебник для 9 — 10 классов средней школы. Под ред. Ю. И. Полянского. Изд. 17-е, перераб. — М.: Просвещение, 1987. — 288с.
- ↑ А. Н. Несмеянов, Н. А. Несмеянов. Начала органической химии. Книга вторая 221. Архівавана з першакрыніцы 27 снежня 2012. Праверана 26 снежня 2012.
- ↑ Collier 1998, pp. 96–99.
- ↑ Tropp 2012, pp. 5–9.
Літаратура[правіць | правіць зыходнік]
- Collier, Leslie; Balows, Albert; Sussman, Max. Topley and Wilson’s Microbiology and Microbial Infections / Mahy, Brian and Collier, Leslie. Arnold. — ninth edition. — Virology, 1998. — Т. 1. — ISBN 0-340-66316-2.
- Hunter, Graeme K. Vital Forces: The Discovery of the Molecular Basis of Life. — San Diego: Academic Press, 2000. — ISBN 0-12-361810-X.
- Tropp, Burton E. Molecular Biology. — 4th. — Jones & Bartlett Learning, 2012. — ISBN 978-1-4496-0091-4.
- Беларуская энцыклапедыя: У 18 т. Т. 3: Беларусы — Варанец / Рэдкал.: Г. П. Пашкоў і інш. — Мн. : БелЭн, 1996. — Т. 3. — 511 с. — 10 000 экз. — ISBN 985-11-0035-8. — ISBN 985-11-0068-4 (т. 3).
- Березов Т. Т., Коровкин Б. Ф. Биологическая химия: Учебник. — 3. — М.: Медицина, 1998. — 704 с. — ISBN 5-225-02709-1.
- Біяхімія // Беларусь: энцыклапедычны даведнік / Рэдкал. Б. І. Сачанка (гал. рэд.) і інш.; Маст. М. В. Драко, А. М. Хількевіч. — Мн.: БелЭн, 1995. — С. 118. — 800 с. — 5 000 экз. — ISBN 985-11-0026-9.
Спасылкі[правіць | правіць зыходнік]
 На Вікісховішчы ёсць медыяфайлы па тэме Біяхімія
На Вікісховішчы ёсць медыяфайлы па тэме Біяхімія- Відэаматэрыялы па біяхіміі
- Molecular Cell Biology
